Grundprinzipien von Batterien
Batterien sind grundlegende Bestandteile moderner Technologie und finden Anwendung in einer Vielzahl von Geräten, von Mobiltelefonen bis hin zu Elektroautos. Ihre Funktionsweise basiert auf elektrochemischen Prozessen, die es ermöglichen, chemische Energie in elektrische Energie umzuwandeln. Im Folgenden wird das grundlegende Prinzip der Funktionsweise von Batterien erläutert.
Die Elektrochemische Zelle
Das Herzstück einer Batterie ist die elektrochemische Zelle, in der spontane Redoxreaktionen stattfinden. Diese Zellen bestehen aus zwei Elektroden – der Anode und der Kathode – die durch einen Elektrolyten getrennt sind. Der Elektrolyt ist eine ionisch leitfähige, aber elektrisch isolierende Substanz.
Speicherung chemischer Energie
Chemische Energie wird in Batterien durch Metalle wie Zink (Zn) oder Lithium (Li) gespeichert. Diese Metalle sind aufgrund ihrer hohen Energie und des Fehlens einer Stabilisierung durch d-Elektronenbindung besonders geeignet. So kann beispielsweise Lithium eine hohe spezifische Kapazität von \( 3,86 \, \text{Ah/g} \) und ein extrem niedriges Elektrodenpotential von \( -3,04 \, \text{V} \) gegenüber der Standard-Wasserstoffelektrode aufweisen.
Oxidations-Reduktions-Reaktion
Alle Batterietypen, unabhängig von ihrer Materialzusammensetzung, nutzen das Prinzip der Oxidations-Reduktions-Reaktion. Bei dieser Reaktion werden Elektronen von einem Element zum anderen übertragen, was zu einer Änderung des Oxidationszustands der beteiligten Atome führt. Dies führt zur Oxidation des Anodenmaterials (Elektronenabgabe) und zur Reduktion des Kathodenmaterials (Elektronenaufnahme).
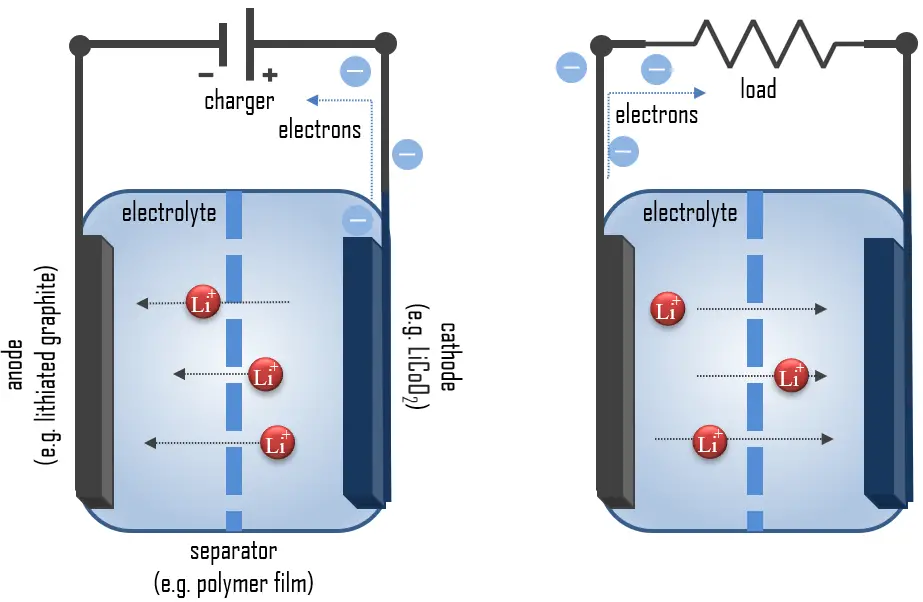
Funktionsweise von Lithium-Ionen-Batterien
Bei Lithium-Ionen-Batterien wandern während der Entladung Lithiumionen von der Anode zur Kathode und umgekehrt während des Ladevorgangs. Dieser Prozess kann durch die folgenden chemischen Reaktionen beschrieben werden:
Entladung: \( \text{C}_6\text{Li} \rightarrow 6\text{C}(\text{Graphit}) + \text{Li}^+ + \text{e}^- \)
Ladung: \( 6\text{C}(\text{Graphit}) + \text{Li}^+ + \text{e}^- \rightarrow \text{C}_6\text{Li} \)
Schlussfolgerung
Batterien sind somit wesentliche Quellen von Gleichstrom (DC) und konvertieren gespeicherte chemische Energie in elektrische Energie. Diese Umwandlung ermöglicht das Fließen von Strömen in elektrischen und elektronischen Schaltkreisen und stellt damit eine entscheidende Komponente in der modernen Technologie dar.