電池の動作原理
電池は化学エネルギーを電気エネルギーに変換する装置であり、その基本原理は、イオン伝導性がありながら電気的に絶縁された物質である電解質によって分離された二つの電極間で起こる自発的な酸化還元反応に基づいています。例えば、ZnやLiのような高エネルギー金属に化学エネルギーが貯蔵されるのは、これらがd電子結合によって安定化されないためです。遷移金属とは異なります。電池にはさまざまな種類が存在し、異なる材料の組み合わせが用いられますが、すべてが酸化還元反応の同じ原理を使用しています。
電池は、エネルギー的に有利な酸化還元反応が外部回路を通じて電子が移動するときにのみ発生するように設計されています。簡単に言えば、各電池はカソードとアノードを分離して反応を防ぐように設計されています。貯蔵された電子は回路が閉じたときにのみ流れます。これは、電池が装置に設置され、装置がオンにされたときに起こります。電気化学過程を通じて貯蔵された化学エネルギーを電気エネルギーに変換することで、DC電気エネルギーの源となります。これにより、電気および電子回路で電流が流れるための起電力を提供します。典型的な電池は一つ以上のボルタ電池から構成されます。
酸化還元反応は、関与する原子の酸化状態に変化をもたらす化学反応です。一方の元素から別の元素へ電子が移動します。その結果、ドナー元素(アノード)は酸化され(電子を失う)と、レシーバー元素(カソード)は還元され(電子を得る)ということになります。例えば、ダニエル電池は異なる金属の二つの電極、ZnとCuで構成され、各電極は自身のイオンの溶液、亜鉛硫酸と銅硫酸と接触しています。ダニエル電池で起こる酸化還元反応は以下の通りです:
この過程はカソードに固体銅の蓄積と、溶液中の亜鉛イオンとしての亜鉛電極の腐食をもたらします。亜鉛金属の酸化によって生成される余分な電子はアノードから「押し出され」、ワイヤーを通じて旅をし、銅カソードに「引き込まれ」そこで銅イオンの還元によって消費されます。電気的な電流は電位差と起電力を引き起こします。銅よりも亜鉛がより優れた還元剤であり、より多くの電子を放出する能力があるため、自発的な反応が起こります。アノードでの電子の放出能力が強いほど、強い起電力が引き起こされます。
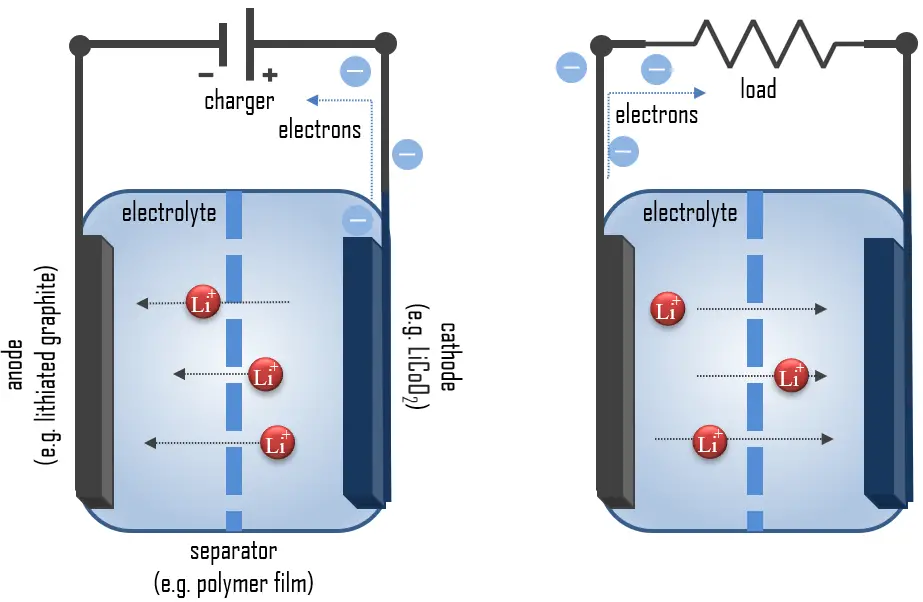
リチウムイオン電池の動作原理
リチウム金属は最も軽い金属であり、高い比容量(3.86 Ah/g)と極めて低い電極電位(−3.04 V vs. 標準水素電極)を持っているため、高電圧および高エネルギー電池にとって理想的なアノード材料です。放電時、リチウムはリチウムグラファイトアノード内でLiからLi+(0から+1の酸化状態)へ酸化され、以下の反応を経て行われます: C6Li → 6C(グラファイト) + Li+ + e–。これらのリチウムイオンは電解質媒体を通ってカソードに移動し、リチウムコバルト酸化物に組み込まれることで、コバルトが+4から+3の酸化状態に還元される次の反応が起こります: CoO2 (s) + Li+ + e– → LiCoO2 (s)。これらの反応は、セルを再充電するために逆方向で実行することができます。この場合、リチウムイオンはリチウムコバルト酸化物カソードを離れ、アノードに戻って移動し、そこで中性リチウムに還元されてグラファイトネットワークに再組み込まれます。