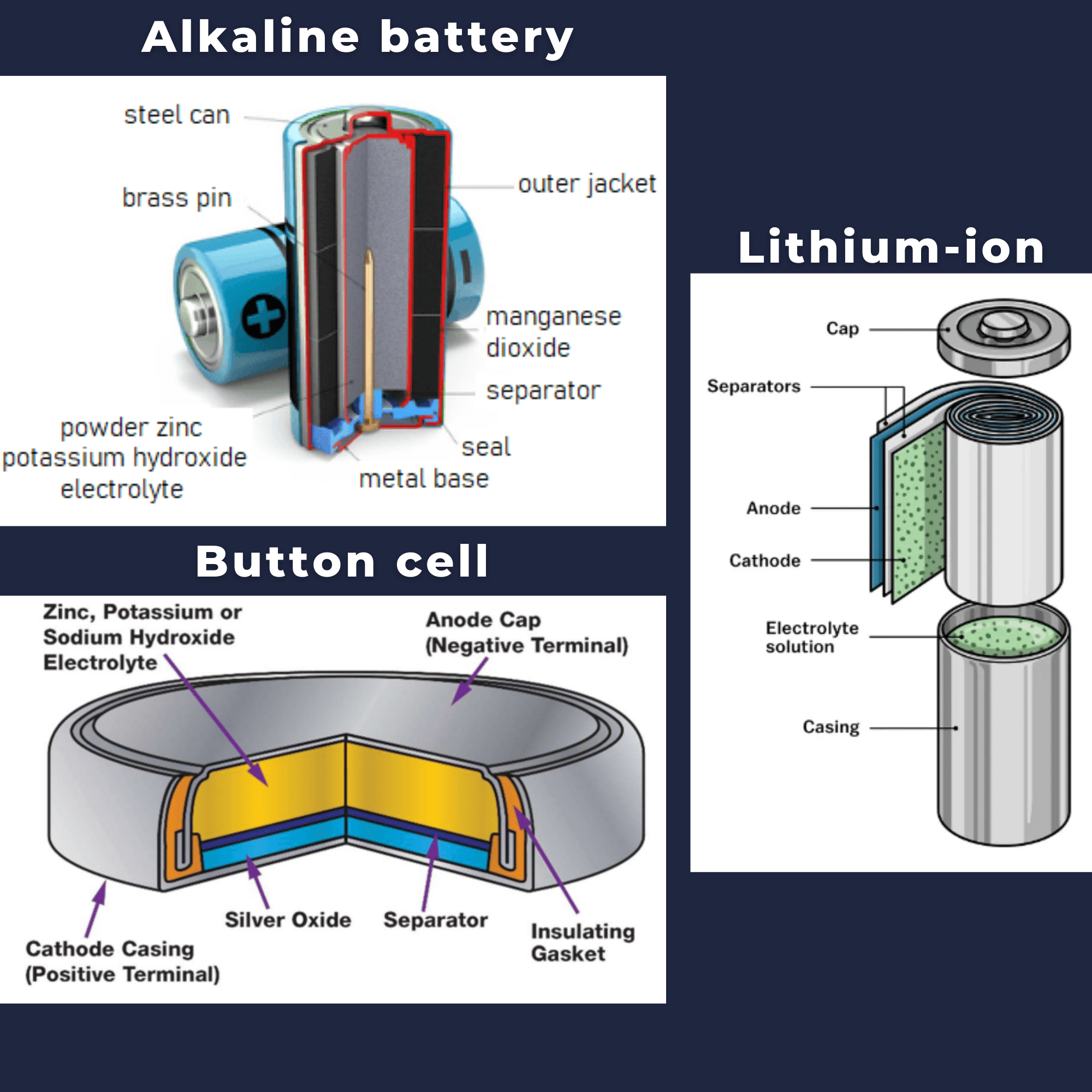
電池の構成要素
電池は、鉛、ニッケル、亜鉛、リチウムなど、多種多様な材料で作られており、それぞれが電池の機能性や性能に異なる特性をもたらします。電池の化学的及び材料的構成は、そのサイズ、形状、全体的な性能を決定します。したがって、各電池は異なる構成を持っていますが、材料の組成が異なる場合でも、ほとんどの電池にはいくつかの共通のコンポーネントがあります。
主な部品は以下の通りです。
– カソード(陽極)
– アノード(陰極)
– 電解質
– セパレータ
– 電流コレクター
電池は、蓄えられた化学エネルギーを電気エネルギーに変換する電気化学的プロセスを通じて、電気及び電子回路に電流を流すための起電力を提供する直流(DC)電気エネルギーの源です。
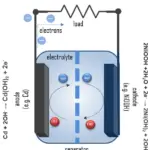
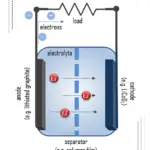
電気化学セルの基本原理
電気化学セルの基本は、電解質によって分離された二つの電極で自発的な酸化還元反応が起こることです。電解質はイオンが電気を伝導するが電子を伝導しない物質です。化学エネルギーは、例えば高エネルギー金属であるZnやLiに蓄えられます。これらは遷移金属と異なりd電子結合によって安定化されていないためです。多くの種類の電池が異なる材料の組み合わせで存在しますが、すべての電池は酸化還元反応の同じ原理を使用しています。
電池の種類とその構成
電気化学セルには、ガルバニックセル、電解セル、燃料セル、フローセル、ボルタ電池など、さまざまな化学プロセスとデザインのセルがあります。湿式セル電池には液体電解質があり、乾式セルは電流が流れるのに十分な湿度のペースト状電解質を使用します。電池の化学的及び材料的構成は、そのサイズ、形状、全体的な性能を決定します。
電池の主要部品
– カソード:カソードは正極または酸化電極で、外部回路から電子を獲得し、電気化学反応中に還元されます。リチウム電池の場合、カソード材料は一般にLiCoO2またはLiMn2O4で構成されます。
– アノード:アノードは負極または還元電極で、外部回路に電子を放出し、電気化学反応中に酸化されます。現在、最も一般的なアノード材料はリチウムでインターカレートされたグラファイト、LixC6です。
– 電解質:電解質はイオンを含む媒体であり、これらのイオンの移動によって電気を伝導しますが、電子は伝導しません。リチウムイオン電池の電解質は、通常、有機溶媒に溶解したリチウム塩です。
– セパレータ:セパレータは、電池のアノードとカソードの間に配置された透過性膜です。セパレータの主な機能は、二つの電極を電気的な短絡を防ぐために分離することと、電気化学セル内での電流の通過中に必要なイオン荷電キャリアの輸送を可能にすることです。
– 電流コレクター:電流コレクターは、電極から外部回路への電子の流れを転送するための電池コンポーネントです。
電池の特性
各電池を比較し理解するために、各電池固有のいくつかの重要なパラメータがあります。これらのパラメータは、特定の要件がある場合に必要な電池を選択する際の参照点となります。電池はあらゆる種類のデバイスに使用され、無限の目的のために使用されます。
– セル電圧:電気化学反応における正極と負極の材料の電位差によって生成されます。
– カットオフ電圧:最小許容電圧であり、通常、電池の「空」状態を定義する電圧です。
– 容量:電池が特定の放電電流で100% SOCからカットオフ電圧まで放電したときに利用可能な総アンペア時数です。
– Cレート:電池の放電速度を表します。
– 自己放電:電池は接続されて電流を供給していなくても徐々に自己放電します。
– 劣化:充電放電サイクルごとに充電式電池の一部の劣化が発生します。
– 放電深度:電池から引き出されたエネルギーの量を、全容量の割合として表したものです。
– 充電状態:電池に残っているアンペア時数量に相当する、定義された「満充電」と「空」状態に関連する電池の充電量です。