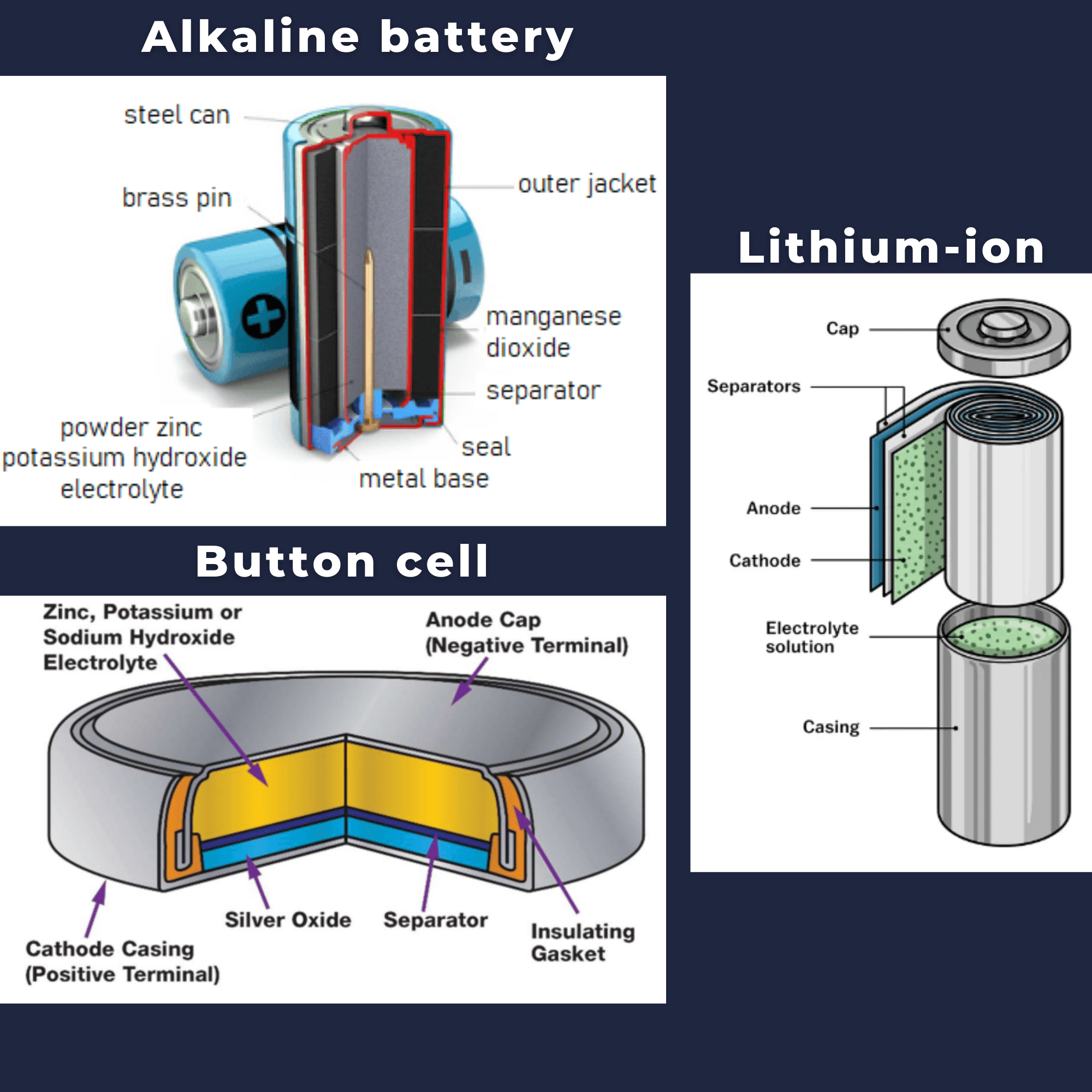
Composition des Batteries
Les batteries, sources essentielles d’énergie électrique continue, transforment l’énergie chimique stockée en énergie électrique grâce à un processus électrochimique. Leur composition, variée et complexe, influence directement leur taille, format et performances globales.
Matériaux Communs des Batteries
Les batteries sont constituées de divers matériaux tels que le plomb, le nickel, le zinc et le lithium. Chaque type possède des caractéristiques uniques, adaptées à des applications spécifiques. Par exemple, le zinc ou le lithium sont privilégiés pour leur haute énergie, contrairement aux métaux de transition stabilisés par des liaisons d’électrons.
Principe de Fonctionnement
Le cœur d’une batterie est la cellule voltaïque. Elle fonctionne sur le principe des réactions d’oxydo-réduction spontanées entre deux électrodes, séparées par un électrolyte. Ce dernier est un conducteur ionique mais un isolant électrique. Les réactions chimiques permettent le stockage de l’énergie et sa conversion en énergie électrique.
Types de Batteries
On distingue plusieurs types de cellules électrochimiques, dont les cellules galvaniques, électrolytiques, à combustible, à flux et les piles voltaïques. Parmi elles, les batteries humides avec électrolyte liquide et les batteries sèches à électrolyte en pâte se distinguent par leur construction et applications.
Composants Clés d’une Batterie
Une batterie typique comprend plusieurs composants essentiels :
- Cathode : Électrode positive où se produisent les réactions de réduction. Les cathodes de batteries au lithium sont souvent en LiCoO2 ou LiMn2O4.
- Anode : Électrode négative où se déroulent les réactions d’oxydation. L’anode en graphite lithié, LixC6, est couramment utilisée.
- Électrolyte : Milieu conducteur ionique, crucial pour la performance et la sécurité. Dans les batteries lithium-ion, il s’agit souvent d’un sel de lithium dissous dans des solvants organiques.
- Séparateur : Membrane perméable entre anode et cathode, empêchant les courts-circuits tout en permettant le transport des ions.
- Collecteurs de courant : Composants transférant les électrons des électrodes au circuit externe. Les feuilles métalliques minces sont préférées pour réduire la taille et améliorer la capacité volumétrique.
Caractéristiques des Batteries Électriques
Plusieurs paramètres sont cruciaux pour comparer les batteries :
- Tension de la Cellule : Différence de potentiel entre les matériaux des électrodes.
- Tension de Coupure : Tension minimale définissant l’état « vide » de la batterie.
- Capacité : Quantité totale d’Ampères-heures disponibles lors de la décharge.
- Taux de C : Taux de décharge exprimé en C.
- Auto-décharge : Perte progressive de charge même sans connexion au circuit.
- Dégradation : Détérioration sur chaque cycle de charge-décharge.
- Profondeur de Décharge : Mesure de l’énergie retirée de la batterie.
- État de Charge : Quantité de charge restante dans la batterie.
FAQ sur les Batteries
Quels sont les principaux composants d’une batterie ? Anode, cathode, électrolyte et séparateur.
Pourquoi les batteries alcalines sont-elles de 1,5 V et les rechargeables de 1,2 V ? Cela est dû à leurs chimies différentes. Les cellules primaires baissent progressivement de tension, alors que les cellules secondaires maintiennent une tension plus uniforme.
Quelle est la différence entre les batteries lithium-ion et lithium-polymère ? Les batteries Li-polymère utilisent un électrolyte en gel polymère hautement conducteur, une évolution des batteries lithium-ion et lithium-métal.