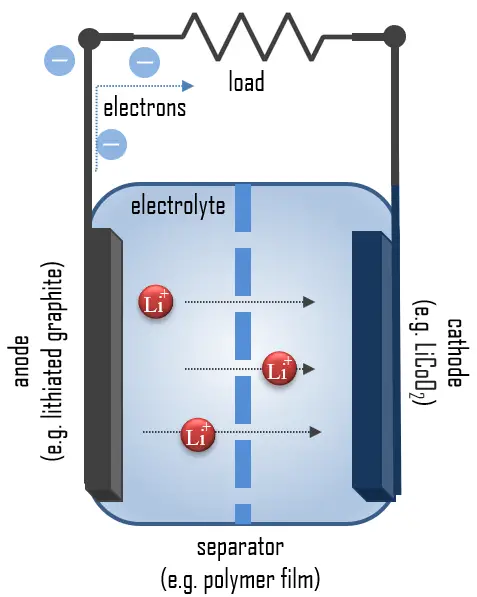
배터리 방전에 관한 이해
배터리 방전은 회로가 닫혀 있을 때 발생합니다. 예를 들어 리튬 이온 배터리에서는 캐소드(음극, 예: LiCoO2)가 전자를 더 강하게 끌어당겨 아노드(양극, 예: 리튬-그래파이트)에서 회로 내의 전선을 통해 전자를 캐소드 전극으로 이동시킵니다. 이 과정에서 각 배터리는 전압을 잃게 됩니다. 이 배터리 화학 반응, 즉 전선을 통한 전자의 흐름이 바로 전기입니다.
C-레이트와 배터리 용량
C-레이트는 배터리가 최대 용량에 비례하여 방전되거나 충전되는 속도를 나타냅니다. 단위는 h-1입니다. 배터리의 쿨로메트릭 용량은 100% SOC에서 컷오프 전압까지 특정 방전 전류로 배터리를 방전할 때 사용할 수 있는 총 암페어-시간입니다. 전기 배터리는 본질적으로 DC 전기 에너지의 원천입니다. 이는 저장된 화학 에너지를 전기화학 과정을 통해 전기 에너지로 변환합니다. 이로써 전기 및 전자 회로에서 전류가 흐르는 데 필요한 전기기전력을 제공합니다. 전형적인 배터리는 하나 이상의 전지로 구성됩니다.
배터리 방전의 화학
간단히 말해, 각 배터리는 캐소드와 아노드를 분리하여 반응을 방지하도록 설계되었습니다. 저장된 전자는 회로가 닫혔을 때만 흐릅니다. 이는 배터리가 장치에 배치되고 장치가 켜질 때 발생합니다. 배터리는 화학 에너지를 전기 에너지로 직접 변환합니다. 예를 들어, 화학 에너지는 Zn 또는 Li와 같은 고에너지 금속에 저장될 수 있습니다. 리튬 금속은 가장 가벼운 금속이며 높은 비용량(3.86 Ah/g)과 매우 낮은 전극 전위(-3.04 V 대 표준 수소 전극)를 가지고 있어 고전압 및 고에너지 배터리에 이상적인 아노드 재료입니다.
배터리의 용량과 자가 방전
다양한 배터리 화학 및 크기는 다른 셀 전압 및 용량을 만듭니다. 예를 들어, CR2032 배터리는 리튬 망간 산화물 기술을 사용하여 3V의 명목 전압과 210mAh의 용량을 제공합니다. 이 코인 셀은 지름이 20mm이고 두께가 3.2mm입니다.
배터리는 연결되어 전류를 공급하지 않아도 점차적으로 자가 방전됩니다. 이는 셀 내부에서 부하가 적용되지 않을 때도 발생하는 비전류 생성 “측면” 화학 반응 때문입니다. 배터리를 낮은 온도에서 저장하면 부반응의 속도가 감소하지만, 일부 배터리는 동결로 인해 손상될 수 있습니다. 나이가 많은 충전식 배터리는 일회용 알카라인 배터리보다 빠르게 자가 방전되며, 특히 니켈 기반 배터리가 그렇습니다.
배터리의 기타 특성
각 배터리의 능력을 비교하고 이해하기 위해, 각 배터리는 또한 배터리 유형 내에서도 특정한 중요한 매개변수를 가지고 있습니다. 이러한 매개변수는 배터리가 필요하고 특정한 특성이 요구될 때 참조됩니다. 전지 전압, 컷오프 전압, 용량, C-레이트, 자가 방전, 열화, 방전 깊이, 충전 상태 등이 이에 해당합니다.
각 매개변수는 배터리의 상태를 평가하고 최적의 성능을 유지하는 데 중요한 역할을 합니다.