バッテリー放電について
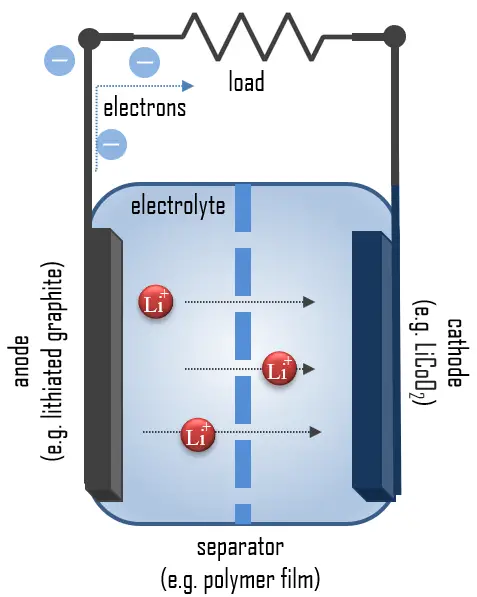
バッテリーの放電は、回路が閉じられたときに発生します。例えばリチウムイオン電池では、陽極(例:リチウム-グラファイト)からカソード(例:LiCoO2)へと、電子が回路の中のワイヤーを通って引き寄せられます。この過程で、各バッテリーは電圧を失います。この化学反応、すなわち電子の流れは電気です。
Cレートとは
Cレートは、バッテリーがその最大容量に対してどれくらいの速さで放電または充電されるかを表す指標です。単位はh−1です。バッテリーのクーロン容量は、100% SOCからカットオフ電圧までの特定の放電電流で放電されたときの総アンペア時間です。
バッテリーの化学
各バッテリーは、陽極とカソードを分離して反応を防ぐように設計されています。電子が流れるのは回路が閉じられたとき、つまりバッテリーが装置に設置され、装置がオンになったときです。バッテリーは化学エネルギーを直接電気エネルギーに変換します。例えば、ZnやLiなどの高エネルギー金属に化学エネルギーが蓄えられます。リチウムは非常に軽く、高い比容量(3.86 Ah/g)と非常に低い電極電位(−3.04 V 対標準水素電極)を持つため、高電圧および高エネルギーのバッテリーに最適な陽極材料です。放電時、リチウムはリチウム-グラファイト陽極で次の反応を通じてLiからLi+(酸化状態0から+1)に酸化されます:
C6Li → 6C(グラファイト) + Li+ + e−
これらのリチウムイオンは電解質媒体を通ってカソードへ移動し、次の反応でリチウムコバルト酸化物に取り込まれます:
CoO2 (s) + Li+ + e− → LiCoO2 (s)
バッテリーの容量
バッテリーのクーロン容量は、特定の放電電流で100% SOCからカットオフ電圧まで放電されたときの総アンペア時間です。これは、含まれる活性物質の量によって決まり、バッテリーから抽出できる最大量の電気化学エネルギーを表します。異なるバッテリーの化学とサイズは異なる電池電圧と容量を生み出します。
バッテリーの自己放電
バッテリーは、接続されて電流を供給していなくても、徐々に自己放電します。これは、負荷がかからない状態でもセル内で発生する非電流生成「サイド」化学反応によるものです。サイド反応の速度は、低温で保存されたバッテリーの場合に低下しますが、一部のバッテリーは凍結によって損傷を受ける可能性があります。
その他の特性
電池の性能を比較・理解するためには、各電池の特有のいくつかの重要なパラメータがあります。これらのパラメータは、特定の品質が必要な場合に電池を選択する際の参照点となります。バッテリーはあらゆる種類の装置で無限の目的のために使用されています。