Die Batterieanode: Ein Eckpfeiler der Elektrochemie
Die Anode ist die negative oder reduzierende Elektrode, die Elektronen an den externen Stromkreis abgibt und während einer elektrochemischen Reaktion oxidiert. Ein häufig verwendetes Anodenmaterial in der heutigen Zeit ist lithiiertes Graphit, LixC6, das aus Graphitschichten besteht, die mit Lithium interkaliert sind. Neue Materialien wie auf Silizium basierende und andere Elementmischungen werden erforscht. Lithiiertes Graphit besitzt eine Einheitszelle mit einer HCP-Struktur.
Zusammensetzung von Batterien
Batterien bestehen aus einer Vielzahl von Materialien, die zu unterschiedlichen Fähigkeiten und Verhaltensweisen in der Funktionalität der Batterie führen. Die gängigsten sind Blei, Nickel, Zink und Lithium, jedes mit unterschiedlichen Leistungsmerkmalen und spezifisch für verschiedene Zwecke je nach Anforderungen. Es wurden viele Arten von elektrochemischen Zellen hergestellt, mit unterschiedlichen chemischen Prozessen und Designs, einschließlich galvanischer Zellen, Elektrolysezellen, Brennstoffzellen, Flusszellen und Voltaischen Säulen.
Wet Cell gegen Dry Cell
Eine Nasszellenbatterie verfügt über einen flüssigen Elektrolyten. Andere Namen sind „flooded cell“, da die Flüssigkeit alle internen Teile bedeckt, oder „vented cell“, da bei Betrieb entstehende Gase in die Luft entweichen können. Nasszellen waren Vorläufer der Trockenzellen und werden häufig als Lehrmittel für Elektrochemie verwendet.
Eine Trockenzelle verwendet einen pastenförmigen Elektrolyten mit nur genug Feuchtigkeit, um den Stromfluss zu ermöglichen. Im Gegensatz zu einer Nasszelle kann eine Trockenzelle in jeder Orientierung betrieben werden, ohne zu verschütten, da sie keine freie Flüssigkeit enthält, was sie für tragbare Geräte geeignet macht.
Kathode und Anode
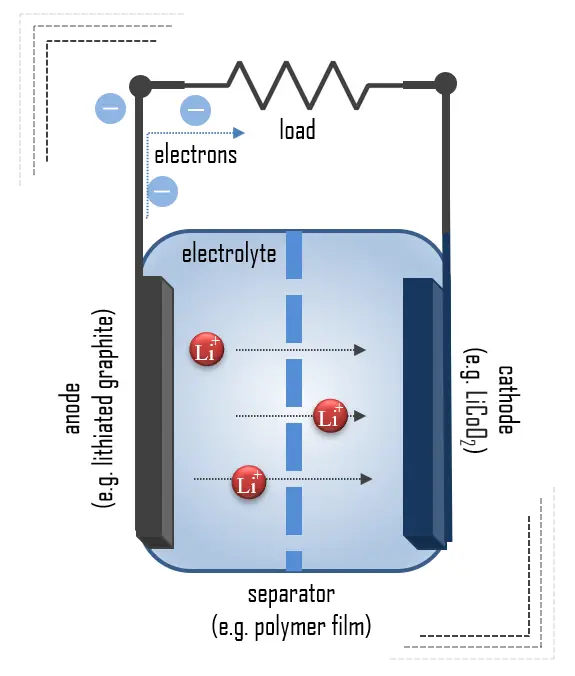
Die Kathode ist die positive oder oxidierende Elektrode, die Elektronen aus dem externen Stromkreis aufnimmt und während der elektrochemischen Reaktion reduziert wird. Bei Lithiumbatterien bestehen die Kathodenmaterialien in der Regel aus LiCoO2 oder LiMn2O4. Wichtig für die Kathode ist, dass sie eine große Menge Lithium ohne signifikante Strukturänderung halten kann, eine gute chemische und elektrochemische Stabilität mit dem Elektrolyt besitzt, ein guter elektrischer Leiter und Diffusor für Lithiumionen ist und kostengünstig ist.
Die Anode ist die negative oder reduzierende Elektrode, die Elektronen an den externen Stromkreis abgibt und während einer elektrochemischen Reaktion oxidiert. Ein häufig verwendetes Anodenmaterial in der heutigen Zeit ist lithiiertes Graphit, LixC6, das aus Graphitschichten besteht, die mit Lithium interkaliert sind. Neue Materialien wie auf Silizium basierende und andere Elementmischungen werden erforscht.
Elektrolyt und Separator
Ein Elektrolyt ist ein Medium, das Ionen enthält und elektrisch leitend ist durch die Bewegung dieser Ionen, jedoch keine Elektronen leitet. Der Batterieelektrolyt ist eine Lösung in Batterien. Abhängig von der Art der Batterie kann es sich um eine flüssige oder pastenartige Substanz handeln. Die Wahl des Elektrolyts in allen Batterien ist entscheidend für Leistung und Sicherheit. In Lithium-Ionen-Batterien ist der Elektrolyt typischerweise ein in organischen Lösungsmitteln gelöstes Lithiumsalz.