自動車用バッテリーの仕組み
自動車用バッテリー、またはSLIバッテリーとも呼ばれる、は自動車を始動させるために使用される充電式バッテリーです。SLIとは、始動(Starting)、照明(Lighting)、点火(Ignition)の頭文字を取ったものです。主な目的は、電動スターターモーターに電流を供給し、それによって化学的に動力を得る内燃エンジンを始動させることです。エンジンが稼働し始めると、車の電気システムへの電力供給はバッテリーによって継続され、需要の増減に応じてオルタネーターがバッテリーを充電します。
自動車用バッテリーは、短時間で最大の電流を供給できるように設計されており、電圧を一定に保ちます。そのため、非常に低い内部抵抗を持っています。これらのバッテリーは、浅いサイクル条件下では良好な寿命を持ちますが、深いサイクル(約12-15サイクル)では寿命が非常に短くなります。
車用バッテリーの化学
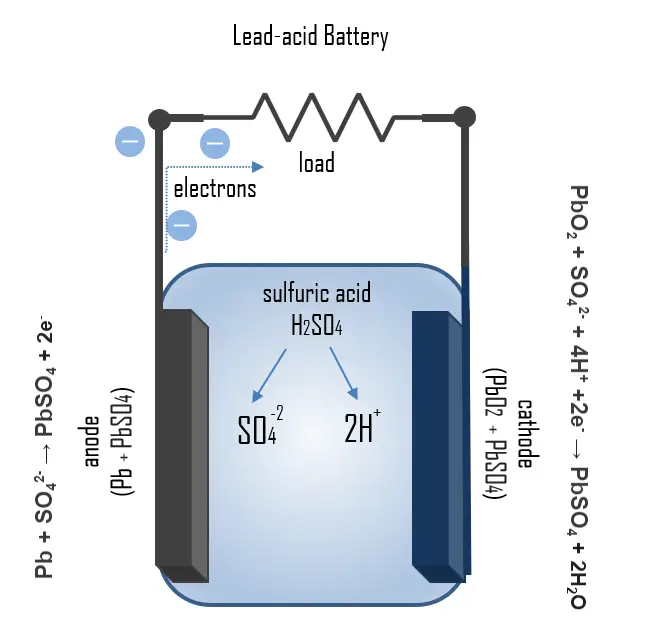
車用バッテリーの動作原理は、充電と放電の間に発生する化学プロセスによって説明できます。放電中、陽極でのプロセスはPb + SO42- → PbSO4 + 2e–となります。鉛は電解質と酸化して硫酸鉛を形成し、二つの電子を放出します。陰極でも硫酸鉛が形成されますが、PbO2 + SO42- + 4H+ +2e– → PbSO4 + 2H2Oの反応で、酸化鉛の還元が行われます。
放電プロセス中に硫酸が使用されるため、電解液の密度を測定することでSoC(充電状態)を決定できます。充電中、放電中に形成された硫酸鉛は鉛と酸化鉛にそれぞれ酸化され、還元されます。硫酸鉛が完全に消費され、充電プロセスが停止しない場合、電解液の電気分解が始まります。過充電により、高い充電電圧が水の電気分解を引き起こし、酸素と水素ガスが発生して逃げます。
密閉型バッテリーでは、ベントの上に触媒(Pd、Pt)があり、発生した水素ガスが水に再結合します。この際の電池電圧は、ガルバニ電位系から決定できます。したがって、この酸化還元反応の総電圧はE0 = 1.68V – (-0.36V) = 2.04Vです。自動車バッテリーの一般的な電圧は12ボルト(DC)ですが、このバッテリーは六つの2V鉛セルから構成されています。