Alkaline Batterien: Eine Übersicht
Alkaline Batterien, bekannt unter dem IEC-Code L, sind primäre Batterien, die elektrischen Strom aus der elektrochemischen Reaktion zwischen Zink und Manganoxid (MnO2) in Gegenwart eines alkalischen Elektrolyten liefern. Sie sind ein weit verbreitetes Produkt und unerlässlich für den Betrieb vieler tragbarer Geräte, wie Werkzeuge, Radios, Spielzeuge und Fernbedienungen. Die gängigste Größe ist die bekannte AA-Batterie. Alkaline Batterien haben eine höhere Energiedichte als wiederaufladbare Sekundärzellen.
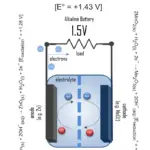
Gesamtreaktion: Zn(s) + 2MnO2(s) ⇌ ZnO(s) + Mn2O3(s) [e° = +1.43 V]
Grundlagen der Elektrochemie in Batterien
Ein elektrischer Akkumulator ist im Wesentlichen eine Quelle elektrischer DC-Energie. Er wandelt gespeicherte chemische Energie durch einen elektrochemischen Prozess in elektrische Energie um. Eine typische Batterie besteht aus einer oder mehreren voltaischen Zellen. Das grundlegende Prinzip in einer elektrochemischen Zelle sind spontane Redoxreaktionen in zwei durch einen Elektrolyten getrennten Elektroden. Der Elektrolyt ist eine Substanz, die ionisch leitfähig und elektrisch isolierend ist.
Zusammensetzung und Chemie der Alkaline Batterien
Die Alkaline Batterie besteht aus fünf Teilen:
- Innenleiter (Stift)
- Anode: Aktives Material ist Zn mit einem Standard-Elektrodenpotential (SEP) von −0.76 Volt.
- Separator: Eine durchlässige Membran zwischen Anode und Kathode.
- Kathode: Aktives Material ist Manganoxid.
- Elektrolyt: Wässriges Kaliumhydroxid.
- Außenleiter (Dose)
Die elektrische Leistung der Zn-MnO2 Batterie stammt aus den elektrochemischen Reaktionen der aktiven Materialien von Kathode und Anode. Ein poröser Separator verhindert das Berühren von Kathode und Anode.
Vorteile und Nachteile von Alkaline Batterien
Vorteile: Alkaline Batterien haben eine hohe Energiedichte, lange Lagerzeiten (geringe Selbstentladung) und sind sofort einsatzbereit. Sie sind oft die beste Wahl für Anwendungen mit geringem Energieverbrauch.
Nachteile: Der Hauptnachteil von Alkaline Batterien ist, dass sie nicht wiederaufladbar sind. Ein weiterer Nachteil ist ihre niedrige C-Rate. Auch Hochstromtypen gelten im Vergleich zu wiederaufladbaren Batterien als niedrig.
Charakteristika von Alkaline Batterien
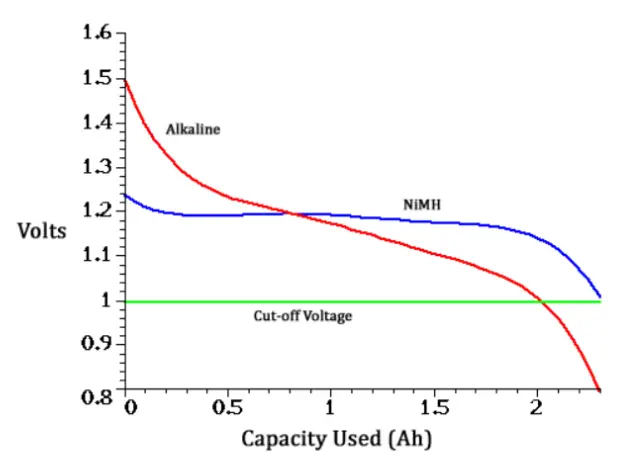
Zellenspannung: Die Spannung von elektrischen Batterien entsteht durch die Potenzialdifferenz der Materialien, die die positiven und negativen Elektroden in der elektrochemischen Reaktion bilden. Alkaline Batterien haben eine offene Zellenspannung von etwa 1,5 V.
Kapazität: Die koulometrische Kapazität ist die gesamte verfügbare Amperestunden, wenn die Batterie mit einem bestimmten Entladestrom von 100% SOC bis zur Abschaltspannung entladen wird. Eine typische alkaline oder NiMH Batterie in der Standardgröße „AA“ hat etwa 2000 bis 3000 mAh (oder 2 bis 3 Ah).
C-Rate der Batterie: C-Rate wird verwendet, um auszudrücken, wie schnell eine Batterie relativ zu ihrer maximalen Kapazität entladen oder geladen wird. Sie hat Einheiten h−1. Eine 1C-Rate bedeutet, dass der Entladestrom die gesamte Batterie in 1 Stunde entlädt.
Häufig gestellte Fragen
Wie lagert man Alkaline Batterien? Alkaline Batterien sind chemisch stabil und haben eine sehr niedrige Selbstentladungsrate. Sie verlieren typischerweise 2 bis 3 Prozent ihrer ursprünglichen Ladung pro Jahr bei Lagerung bei Raumtemperatur (20–30 °C).
Warum lecken Batterien? Alkaline Batterien neigen dazu, Kaliumhydroxid (KOH) auszulaufen, eine ätzende Substanz, die Atemwegs-, Augen- und Hautreizungen verursachen kann. Der Grund für Leckagen ist, dass sich die Chemie der Zellen bei Entladung ändert und etwas Wasserstoffgas erzeugt wird. Wenn eine Batterie für längere Zeit ungenutzt in einem Gerät verbleibt, kann der resultierende Gasdruck das Gehäuse aufbrechen und zu Leckagen führen.