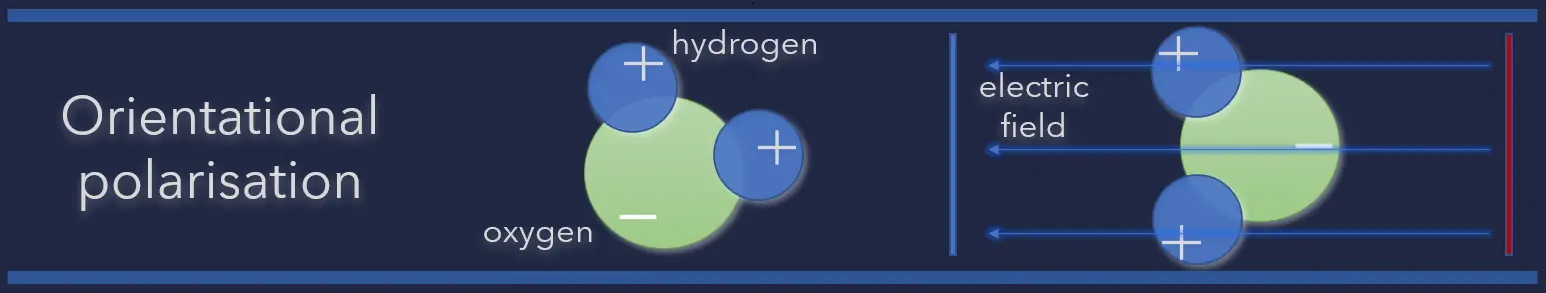
電気分極の基本:指向性分極
電気分極とは、物質内の分子や粒子が外部電場に応じて配列することによって生じる現象です。外部電場がかかると、極性を持つ分子や粒子は電場の方向に合わせて回転し、荷電の分離と双極子モーメントの生成が起こります。これを指向性分極と呼びます。指向性分極の大きさは、電場の強度、分子や粒子の双極子モーメント、および物質の温度などの要因に依存します。この効果は、双極子モーメントが高く温度が低い材料で最も強く現れます。
指向性分極の科学的意義
指向性分極は、材料科学、電気化学、生物物理学など多くの科学分野において重要です。液晶のような物質の挙動においても、この現象は重要な役割を果たします。液晶は、液体と固体の中間的な性質を示す物質で、ディスプレイ技術などの応用分野で重要な役割を担っています。
電気分極とは
金属とは異なり、誘電体内ではすべての電荷が特定の原子や分子に結びついています。これらの電荷は、束縛電荷と呼ばれます。しかし、外部電場の適用によって、これらの電荷は原子内または分子内で変位(分極)されます。電気分極は、外部電場によって誘導された絶縁体または誘電体の原子や分子内での正負の電荷の微小な相対的シフトです。これらの微細な変位は、導体内の電荷の再配列ほど劇的ではありませんが、誘電体の特徴的な振る舞いを説明するために重要です。
分極の種類
分極には三種類があります。
- 電子分極:外部電場が適用されると、原子の電子雲が重い核に対して原子の大きさの範囲内で変位します。これが電子分極です。
- 指向性分極:指向性分極は、分子に固有のものであるか、非対称的な核の歪みが可能な任意の分子に誘導される分極です。極性分子は、正負の分子が衝突する可能性がほとんどまたは全くない誘電体です。これは、それらがすべて非対称な形をしているためです。H2Oは典型的な例です。電場がない場合、これらの分子の電気双極子モーメントは予測不可能な方向に動きます。その結果、平均双極子モーメントは0になります。外部電場がある場合、分子は電場と同じ方向に集まります。
- イオン分極:イオン分極は、例えばNaClのようなイオン結晶内の正と負のイオン間の相対的な変位によって生じる分極です。
このように、指向性分極は物質の電気的性質を理解する上で不可欠な概念であり、多くの応用技術において基本的な役割を果たしています。